標準治療では、患者さんとのコミュニケーションを重視しつつ、抗原除去・回避、アレルゲン免疫療法、薬物療法、手術療法の4つを柱に行います。
- 悩み・目的
- 個別の病気
花粉症と治療法【後編】

花粉症の患者さんは年々増加しており、1998年と2008年で比較すると、有病率は19.6%から29.8%へと1.5倍に上昇しています。つまり、約3割の方が花粉症ということです。花粉症患者さんが増えた理由の一つに、スギ花粉の増加があります。
スギは植林後40年ほどで成木になり、花粉を飛散し始めます。現在、植林されたスギの大半が樹齢40~60年となり、活発に花粉が飛散する時期を迎えています。また、花粉症の主な発症原因は、遺伝的にアレルギー体質であることと言われております。それ以外の原因としては、食生活の変化、生活環境の変化、ストレスなどが挙げられます。
今回は国民病と言われる「花粉症」の標準的な治療法と補完代替療法についてお話ししたいと思います。
※前編はこちらhttps://isom-japan.org/article/article_page?uid=KktEi1581579320
標準的な治療法について
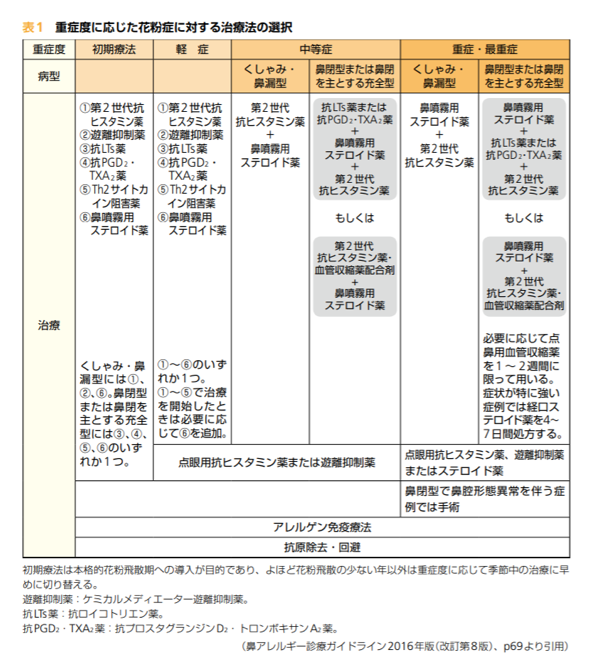
<表>
ⅰ.自然治癒―抗原除去と回避
ⅱ.アレルゲン免疫療法
1)皮下免疫療法(subcutaneous immunotherapy;SCIT)
2)舌下免疫療法(sublingual immunotherapy;SLIT)
ⅲ.薬物療法
1)ケミカルメディエーター遊離抑制薬(マスト細胞安定薬)
2)ケミカルメディエーター受容体拮抗薬
①ヒスタミンH 1 受容体拮抗薬
②ロイコトリエン受容体拮抗薬
③プロスタグランジンD2・トロンボキサンA2受容体拮抗薬
3)Th2サイトカイン阻害薬
4)ステロイド薬
①鼻噴霧用ステロイド薬
②全身ステロイド薬
5)点鼻用血管収縮薬・α交感神経刺激薬
6)その他
①非特異的変調療法薬
②生物製剤
③漢方薬
ⅳ.手術療法
薬物療法について
鼻閉型や特に喘息を合併している場合には、ロイコトリエン受容体拮抗薬が推奨されます。くしゃみ・鼻漏型の重症・最重症例では、鼻噴霧用ステロイド薬と第2世代ヒスタミンH1受容体拮抗薬を併用します。
鼻閉型または鼻閉を主とする充全型の重症・最重症例では、鼻噴霧用ステロイド薬、ロイコトリエン受容体拮抗薬あるいはプロスタグランジンD2・トロンボキサンA2受容体拮抗薬、第2世代ヒスタミンH1受容体拮抗薬の3種類を併用または鼻噴霧用ステロイド薬と第2世代ヒスタミンH1受容体拮抗薬・血管収縮薬配合剤の併用を選択します。
重症の鼻閉がある患者さんでは、点鼻用血管収縮薬の短期間の併用も検討します。ただし、点鼻用血管収縮薬は2歳未満の小児には禁忌であるため、原則として6歳以上の小児および成人に対して用います。例年強い症状を示す患者さんには、花粉飛散時の症状軽減を目的として、初期療法を推奨します。初期療法の開始時期は、使用する薬剤の効果発現に要する時間、患者の例年の花粉飛散に対する過敏性を念頭において決定します。
注)通常、第2世代ヒスタミンH1受容体拮抗薬、ロイコトリエン受容体拮抗薬、鼻噴霧用ステロイド薬は花粉飛散予測日または症状が少しでも現れた時点で開始します。その他の薬剤は効果発現にやや時間がかかるため、花粉飛散予測日の1週間前を目途に開始します。
注)成人で症状が特に強い患者さんにおいては、経口ステロイド薬の短期間(4〜7日)処方で治療を行うことがあります。
注)重症のアレルギー性結膜炎では、ステロイド点眼薬が必要となることもありますが、この場合定期的な眼圧測定が推奨されます。
PETを用いた脳内ヒスタミン受容体占拠率のデータから、占拠率20%以下のヒスタミンH1受容体拮抗薬が推奨されます。脳内ヒスタミン受容体はヒスタミン神経系すなわち学習、覚醒、痙攣抑制に重要な機能を持っているため、鎮静作用の強い抗ヒスタミン薬ではこの重要な機能が抑制される恐れがあります。脳機能を低下させてまでも鎮静作用を有する抗ヒスタミン薬を使用すべきではないと考えられております。
初期療法の作用メカニズムは、抗ヒスタミン薬がヒスタミン受容体の invers agonist として作用する考えが有力です。つまり、ヒスタミン受容体には活性化したものと活性化していないものが平衡状態にあり、抗ヒスタミン薬がヒスタミン受容体に結合すると受容体を不活性化させる働きがあると考えられています。抗原と受容体が結合して活性化するとアレルギー反応が増悪しますが、受容体が不活性化した状態ではアレルギー反応も減弱すると考えられます。4)
アレルゲン免疫療法について
花粉症治療における第一選択は、抗ヒスタミン薬に代表される抗アレルギー薬による薬物療法です。しかし薬物療法は対症療法ですので、花粉症の症状がある限り薬を服用し続ける必要があります。一方、アレルゲン特異的免疫療法(allergen specific immunotherapy:AIT)は、アレルギー疾患に対して根治あるいは長期寛解が期待できる唯一の治療法です。スギ花粉症に対して行われる舌下免疫療法(sublingual immunotherapy:SLIT)には高い安全性があるため、有効な治療法と言えます。
舌下免疫療法の作用機序はまだ十分に解明されておりませんが、アレルゲンに起因するアレルギー反応が減弱されることから、Th2免疫応答が抑制されていると考えられます。舌下投与されたアレルゲンは口腔粘膜下の樹状細胞により補足されて、Th2細胞の減少とTh1細胞の増加、抑制性T細胞の分化および誘導亢進を起こします。AITを行うと、血清中のアレルゲン特異的IgG抗体の産生が増加します。増加したIgG抗体はアレルギーの引き金となるIgE抗体とアレルゲンの結合を競合的に阻害するブロッキング抗体として働き、アレルギー反応を抑制します。
補完代替療法について
補完代替療法(Complementary and alternative medicine : CAM)の内容は様々です。日本国内で行われた調査では漢方(医師の処方によらないもの)、甜茶(てんちゃ。甘みのある中国茶)、鼻スチーム療法、鼻内洗浄、クロレラ、鍼、花粉グミ、シジュウム茶、灸、ツボ、情動水、シジュウム入浴剤、波動水、スギの葉エキスなどが挙げられていました。最近の調査では、ヨーグルト、乳酸菌剤やアロマ療法の増加が目立っております。
アンケートによる治療効果の調査結果は下記の通りです。
【漢方薬】効果あり50%、効果なし35%、不明15%
【甜茶】効果あり14%、効果なし51%、不明35%
【鼻スチーム療法】効果あり46%、効果なし44%、不明10%
患者さん自身の評価では、漢方やスチーム療法などは40%以上の有効率も示されましたが、多くのものは20~30%以下でした。また、有効率が高いものであっても、逆に効果を認めなかったとする割合が高いのも特徴の一つとして見受けられます。鼻スチーム療法は温度を守れば副作用もなく、どうしても薬物治療を受けたくない方や妊婦さんには一時的な効果は期待されます。
使用頻度が増加傾向にあるヨーグルト、乳酸菌剤は、一般医療機関を受診しているアレルギー性鼻炎患者さんの調査では、「効果がある」と判断している方は30%以下でした。
プラセボ効果がみられるアレルギー性鼻炎
アレルギー性鼻炎(花粉症を含む)では、プラセボ効果が高いことが知られています。偽薬が30%を越える高い有効性、すなわちプラセボ効果がみられたという報告もあります。薬物の治療効果を証明するためには盲検試験が必要です。
体への有害成分が含まれていなければ代替療法でも問題はないとも考えられますが、花粉症に効果があるといったことを公言して販売するなら、その疾患に対する有効性を示す必要があります。残念ながら多くのアレルギー性鼻炎に対する代替療法には、十分な効果の根拠が示されていないのが現状です。
栄養療法・サプリメント療法のエビデンス
アレルギー性疾患の有病率が増加している原因としてダイエット仮説があります。日常摂取している食品には、アレルギー疾患の発症に促進的に作用する物質と、抑制的に作用する物質が含まれています。栄養の状態と免疫系の働きには密接な関連がみられ、低栄養、ビタミン類や微量元素の欠乏は適切な免疫機能の保持に支障をきたすことが知られています。
栄養素の欠乏は、自然免疫での食細胞の機能を弱め、サイトカインの生産に影響を与えます。特に①ビタミンA、C、D、E、セレニウム、銅、亜鉛などの抗酸化物質の摂取不足(抗酸化仮説)と②n-3系不飽和脂肪酸(青魚に多く含まれるEPA・DHAなど)に対するn-6系不飽和脂肪酸の摂取過多(脂質仮説)が、アレルギー性疾患増加の一要因であると言われています。
<①についての補足説明>
ビタミンD活性型(1, 25-ジヒドロキシビタミンD3)は、ビタミンAと同様、標的遺伝子の発現を制御する「ステロイドホルモン」として機能します。細胞の核に入る時には、1, 25-ジヒドロキシビタミンD3はVDRに結合して、レチノイドXレセプター(RXR)への結合を促進します。そして、VDR/RXR複合体はビタミンD応答要素(VDREs)として知られているDNAの小さな配列に結合し、特定の遺伝子の転写を調節する数多くの分子間相互作用のカスケードを開始します。
VDRは単球、マクロファージ、樹状細胞、活性化したT細胞を含む数種類の免疫細胞で発現しております。1,25-ジヒドロキシビタミンD3は、自然免疫や獲得免疫の応答を調節することが知られています。また、ビタミンB6はサイトカインや抗体のようなタンパク質の構成単位であるアミノ酸を体内で代謝したり合成する際にも必要となります。
<②についての補足説明>
脂肪酸には免疫応答を調節する作用があります。典型的な欧米型の食事をしている人々では、免疫細胞の細胞膜のアラキドン酸(AA)量はエイコサペンタエン酸(EPA)量を大きく上まわり、その結果として、EPAからよりもAAからのエイコサノイドの形成が大きく上回り、炎症性疾患あるいは自己免疫性疾患を増悪させることになります。したがって、n-3脂肪酸の摂取量を増やすことで、用量依存的に免疫細胞膜のEPA含量を増やすことが可能です。すると、EPAに由来するエイコサノイドがより多く生産され、AAに由来するエイコサノイドが減少します。こうしたメカニズムによりアレルギー性疾患の発症を予防することができるのです。
上述のアレルギー性疾患の発症予防に抗酸化ビタミンや魚油、プロバイオティクスなどによる予防的な効果を検証する報告が多数あります。ビタミンDに関しては、アレルギー性疾患の予防に有効であるという報告が多数なされています。また、ビタミンCには抗ヒスタミン作用があることや、フラボノイドには花粉症の症状緩和に影響を与えるなどの報告もあります。
一方、効果に関しては有意差がないとする否定的な報告もあります。それぞれ適切に計画された学術的な研究であるかどうかを検討すること、そしてその治療法を選択するか否かを検討することが必要だと考えております。
腸内細菌とアレルギー
アレルギー性疾患の増加は、食習慣や住環境といった生活スタイルの変化に起因すると言われていますが、乳幼児期の病原体への暴露がアレルギー性疾患になりにくい免疫学的体質を作るという衛生仮説が提唱されています。従来はTh1/Th2バランスの変化で衛生仮説が説明されてきましたが、最近では腸内細菌の重要性が注目されています。
腸内細菌の定着は、腸管関連リンパ組織を成熟させ、IgA産生を促し、Th17細胞の分化を誘導するなど宿主免疫システムの成熟に必須です。さらに腸内細菌は上皮バリア機能を高めてアレルゲンの侵入を抑制し、炎症やアレルギー反応の制御に関わる制御性T細胞(Treg)を誘導します。乳幼児期における抗生物質の投与や食生活の西洋化が腸内細菌の変容=ディスバイオシスを招き、アレルギー性疾患の発症や増悪につながることが多数報告されております。
プロバイオティクスとは、健康上有益であると考えられる“生きた微生物”です。バクテリアやその他の微生物は有害な「細菌」と考えられがちですが、私たちの身体に生息している多くの微生物は、私たちの身体の機能が適切に働くのを助ける役割を担っています。腸内細菌は食物を消化し、病原菌を殺菌し、そしてビタミンを生成したり免疫システムに働きかけます。
プロバイオティクスとして市販されている製品には食品(ヨーグルトなど)、栄養補助食品、スキンクリームなどの経口でない製品が多数あります。プロバイオティクスが体にとって安全か否かは、個人の健康状態によります。健康な人にとって、プロバイオティクスの副作用が仮に起こるとすれば、通常ガスなどの軽度の消化管症状程度です。しかし、重篤な医学上の問題を抱えている患者さんの場合は、危険な感染症などの副作用が生じるとする報告もあります。
最後に
近年、多くの人々がサプリメントなどの補完代替療法を利用しております。どんな医薬品や治療法、サプリメントであっても、副作用や服用している他医薬品との相互作用がある場合があります。また、反応には個人差があることを注意しなくてはなりません。
安全性や有効性が証明されていない製品を通常の治療の代わりに使用すると、深刻な結果をもたらす可能性もゼロとは言えません。どんな目的でその治療法を選択するのかをよく考え、科学的根拠が得られている治療法を慎重に選択することが重要です。
<参考文献>
- 後藤穣,ガイドラインに基づいたアレルギー性鼻炎,花粉症治療-第2世代抗ヒスタミン薬を中心に-日耳鼻.2019.122.187-191.
- Simons FE, Simons KJ Histamine and H1- antihistamines : celebrating a century of progress. J Allergy Clin Immunol .2011.128 .1139-1150.
- 日本アレルギー学会,スギ花粉症におけるアレルゲン免疫療法の手引.株式会社メディカルレビュー社(2018年7月27日 第2版第1刷発行)
- 岡本美孝,花粉症の民間医療について(厚生労働省)https://www.mhlw.go.jp/new-info/kobetu/kenkou/ryumachi/okamoto.html
- Linus Pauling Institute Micronutrient Information Center. https://lpi.oregonstate.edu/mic
- 統合医療情報発信サイト.厚生労働省https://www.ejim.ncgg.go.jp/pro/overseas/c03/16.html
- 田中敏郎.アレルギー疾患に対する補完代替療法のエビデンス.アレルギー.2012.61(11)1649-1656.
- Carol S. Johnston.The Antihistamine Action of Ascorbic Acid .Subcellular Biochemistry pp 189-213| Cite as
- Hirano T, Kawai M, Arimitsu J, Ogawa M,et al. Preventative Effect of a Flavonoid, Enzymatically Modified Isoquercitrin on Ocular Symptoms of Japanese Cedar Pollinosis. Allergol Int.2009.25;58(3)
- Akbar NA, Zacharek MA.Vitamin D: immunomodulation of asthma, allergic rhinitis, and chronic rhinosinusitis. Curr Opin Otolaryngol Head Neck Surg. 2011 Jun;19(3):224-8. doi: 10.1097/MOO.0b013e3283465687.
- 吉田幸一.アレルギー疾患発症予防-ビタミンDの可能性. 日本小児アレルギー学会誌.2019. 33.3. 308-315.
- Agarwal S, Singh SN, Kumar R, Sehra R. Vitamin D: A Modulator of Allergic Rhinitis.Indian J Otolaryngol Head Neck Surg. 2019 Nov;71(Suppl 3):2225-2230. doi: 10.1007/s12070-019-01697-9. Epub 2019 Jun 27.
- Kanatani KT, Adachi Y, Hamazaki K, et al. Association between vitamin D deficiency and allergic symptom in pregnant women.PLoS One. 2019; 14(4): e0214797.Published online 2019 Apr 10. doi: 10.1371/journal.pone.0214797.
- Ariano R Efficacy of a novel food supplement in the relief of the signs and symptoms of seasonal allergic rhinitis and in the reduction of the consumption of anti-allergic drugs. cta Biomed. 2015 .27.86(1):53-8.
- Sawane K. Nagatake T, Hosomi K.et al Dietary Omega-3 Fatty Acid Dampens Allergic Rhinitis via Eosinophilic Production of the Anti-Allergic Lipid Mediator 15-Hydroxyeicosapentaenoic Acid in Mice. Nutrients. 2019. 22;11(12). pii: E2868. doi: 10.3390/nu11122868.
- 木村五郎,赤木博文,岡田千春 Lactobacillus acidophilus L-55含有ヨーグルト飲用のスギ花粉症に対する臨床効果の検討.アレルギー.2012.61(5)628-641.
- D. P. Strachan: Br. Med. J.1989. 299.1259-1260
- 長谷耕二,大野博司,粘膜免疫系の最前線における上皮細胞の生体防御機構.臨床免疫.2006.29.16-29.
- 松本健治,腸内細菌とアレルギー.小児アレルギー.2010.24.5.669-674
同じタグの記事を読む








